Amadeo Avogadro naceu o 6 de Agosto do 1776 e morreu o 9 de xulio do ano 1856. Foi un físico e químico italiano e profesor de física na universidade de Turin en 1834.
Amadeo Avogadro naceu o 6 de Agosto do 1776 e morreu o 9 de xulio do ano 1856. Foi un físico e químico italiano e profesor de física na universidade de Turin en 1834.
Amadeo era fillo dun avogado, e Amadeo decide seguir o negocio familiar, polo que saca a licenciatura de dereito no ano 1795. Mais tarde inscribese como avogado en Turín, a sua cidade natal. Pero a sua paixon pola fisica e as matemáticas fai que se decida a estudalas. No ano 1809 conseguiu un posto de profesor de física, no colexio real de Vercelli.
- AMADEO AVOGADRO -
3 comentariosNo ano 1811 enuncia a lei de Avogadro ¿porque se chamara asi? moi ben!!!!!!!!!!!!!!!!!!!!!!!!!! porque o quen a enunciou foi Avogadro, ejem, bueno sigamos, Avogadro apoiouse na teoria atómica de Dalton, que a estas alturas xa todos deberiamos coñecer, e na lei de Gay-Lussac(que tamen dimos segun creo recordar) sobre os vectores do movemento da molécula, e descobre que dous volumenes iguais de gases diferentes, nas mesmas condicions de presión e temperatura, conteñen o mesmo número de moléculas. Amadeo envia esta teoria a un xornal francés o 14 de xullo de 1811.
No ano 1820 a universidade de Turin crea para el unha cátedra de física, que ocupara ata sua morte.
En 1841 acaba os seus traballos e os publica en catro tomos có título de 'Fisica dei corpi ponderabili, o trattato della costituzione materiali de corpi' .Puf vaia nomeciño eh?
-O número de Avogadro:
Actualmente, a unidade aceptada polo sistema internacional é o mol, que corresponde a cantidade dunha substancia que contén 6,023 x 10 elevado á 23 , este é o numero de Avogadro.
Espero que vos gustara a entrada .
Daniel Meira.
Publicado por
il Giorgio
en
9:38
![]()
Premio Nobel Física 2007
3 comentariosO outro día (bueno máis ben fai un par de meses), saíu públicado no ABC:
El francés Albert Fert y el alemán Peter Grünberg, Nobel de Física por su descubrimiento de la magneto-resistencia Estocolmo.
El francés Albert Fert y el alemán Peter Grünberg, Nobel de Física por su descubrimiento de la magneto-resistencia Estocolmo.
El francés Albert Fert y el alemán Peter Grünberg son los ganadores del Premio Nobel de Física 2007 por su descubrimiento de la magneto-resistencia, que ha servido para extraer datos de los discos duros de los ordenadores, comunicó hoy la Real Academia de Ciencias de Suecia.
Imos cunha pequena biografía de cada un:
ALBERT FERT
 Albert Fert é un físico francés que naceu fai xa 69 anos ( o 7 de Marzo de 1938) en Carcassonne, Francia (claro, é francés).
Albert Fert é un físico francés que naceu fai xa 69 anos ( o 7 de Marzo de 1938) en Carcassonne, Francia (claro, é francés). Este home que posa tranquilo nesta fotografía pasará á historia por gañalo premio nobel de física no ano 2007, gracias ó descubremento da magnetorresistencia xigante, tema que explicaremos máis abaixo.
É ademáis profesor na Unversité Paris-sud (que ven sendo universidade de paris sur) e director científico dun proyecto moi importante cun centro de investigación dos máis importantes de Francia.
Con isto xa nos chega para saber quen é Albert Fert.
PETER GRÜNBERG
Peter Grünberg é un alemán de 68 anos (un menos que Albert Fert).
Estudiou na Johann Wofgang Goethe Univesität (universidade de Frankfurt para os que non sepan alemán), e despois licenciouse na Universidade Técnica de Darmstadt. Traballou no Forschungszentrum Jülich ( Centro de investigación Jülich).
A este home gústalle descubrir cousas e eso.
¿QUE É A MAGNETORRESISTENCIA XIGANTE?
A magnetoresstencia xigante (GMR para os amigos, que son as siglas do seu nome en inglés - Giant Magnetoresistance-) é un efecto que se produce nunhas esructuras de películas delgadas e que básicamente o que fai é que diminua a resistencia eléctrica, polo que, o que fai é que sea posible almacenar máis datos en menos espacio. Isto fai que o iPod poda ter tanta capacidade, ou que cada vez os discos duros do ordenador teñan máis Gb de memoria (a capacidade dos discos duros aumentou 50 veces grazas a magnetorresistencia xigante)
Aínda que a estes homiños lle acaban de dar o premio nobel de física este ano, isto xa o descubriran no ano 1988.
o sistema que descbriron estes homes foi comercializado por primeira vez en 1997.
o sistema que descbriron estes homes foi comercializado por primeira vez en 1997.
Deixovos aquí un link á traducción da nota que lle otorgaba o premio a Albert Fert e a Peter Grünberg.
HISTORIA DOS PREMIOS NOBEL DE FÍSICA
Os premios nobel de física levan premiando 106 anos os avances nesta disciplina das ciencias.
No ano 1901, o primeiro premio foi para Wilhelm Conrad Röntgen polo descubremento dos raios X
No 1903 a Pierre e Marie Curie polo estudio da radioactividade.
No 1906 a Sir Joseph John Thomson polo seu traballo sobre a conduccion eléctrica dos gases.
1911 a Wilhelmn Wien polodescubremento sobre as leis da radiación do calor.
En 1921 a Einstein pola súa interpretación do efecto fotoeléctrico.
No 1922 a N. Bohr polo estudio da estructura atómica.
1935 a James Chadwick polo descubremento do neutrón.
Poderíamos estar así toda unha larga hora, pero como non vos quero aburrir cunha larga lista dos premios nobel de física, aquí o deixo.
Saudos.
Publicado por
il Giorgio
en
3:58
![]()
- O DIÓXIDO DE CARBONO -
0 comentariosO dióxido de carbono está agora moi de moda por iso do efecto invernadeiro, o cambio climático, ...Pero na súa defensa tamén debemos dicir que non só é un gas malo, senón que tamén o temos, por exemplo, nos extintores para apagalo fuego. Seguro que se se está a quemala túa casa non tre importa que o apretala palanca do extintor estes a contaminar, ¿non?

Como o CO2 é un óxido non metal pois para a súa nomenclatura sistemática comezamos "lendo" dende o final cara o principio.
Para a de Stock poñemos óxido de e o nome do metal. Entre parentesis poñemos a valencia coa que esta actuando.
Neste caso, como temos dous átomos de osíxeno, que actúa coa valencia 2- , o carbono ten que actuar con valencia 4+.
Para a nomenclatura tradicional poñemos a palabra Anhídrido e a continuación a raíz do nome do metal (carbon) e máis o sufixo ico, xa que este metal esta a actuar co número de oxidación máis elevado. Como o carbono ten valencias 2+ e 4+, se actuase con 2+, a menor, poriamos o sufixo -oso.
DATOS SOBRE O DIÓXIDO DE CARBONO
O CO2 atopámolo en estado gas na natureza, xa que ten unha temperatura de ebolución de - 78ºC.
Ten unha masa molecular de 44.01 umas (unidade de masa atómica), que se calula sumando as masas dos átomos que forman a molécula (neste caso, 12.01 do carbono máis 2x16 do osíxeno, xa que temos dos átomos)
CONSECUENCIAS CO2
O CO2 non é precisamente un gas moi bo para a nosa salud nin para o planeta Terra.
Quizais sexa menos peligroso ixestalo que inhalalo (quero dicir que dentro do malo, é menos malo comelo que respiralo, aínda que ambalas dúas cousas son perigosas)
Se tragamos CO2, cousa un pouco dificililla debido a que para ilo, precisaríamos atoparnos a menos de -78ºC baixo cero, provocaríanos nauseas, vómitos e tamén pupita na garganta.
Pero en vez diso, o que si que é moito máis doado de facer é inhalalo, como fixeron os xaponeses durante un tempo, que xuntábanse tres ou catro, metíanse nun coche coas ventanillas pechadas e levaban un tubo dende o tubo de escape ata o interior, de maneira que morrían ó certo tempo, pero iso si, morrían felices, porque o CO2 facía que se durmisen antes de morrer.
Aínda que atopei nunha páxina, que o CO2 non mata. Aquí vos deixo o link:
http://antonuriarte.blogspot.com/2007/01/el-co2-no-mata.html
Creo que o que eu entendín diso non é o que quere dicir, pero ven sendo que no noso alento, hai máis dióxido de carbono que na atmosfera actual.
Pero imos co que esta máis de moda: o cambio climático.
Aínda que non toda a culpa do cambio climático a ten o anhídrido carbónico, gran parte si. Veamos porque.
O CO2 é o gas máis importante dos que provoca o chamado efecto invernadoiro. Contribue nun 55% o calentamento global. Principalmente procede da quema de combustibles fósiles e da deforestación, porque aínda que pareza mentira, as árboles e as plantas, son capaces de transformar o dióxido de carbono en osíxeno.

Unha das causas que me levou a escribir sobre este composto é que o outo día, no programa de Cuatro "El Hormiguero", fixeron unha proposta.
Invitaron a todo o mundo a que plantase unha árbore e se seacase unha foto xunto a ela, Todo isto para loitar contra o efecto invernadoiro. Parece mentira, pero en 13 semanas, xa levan plantados 39.757 árbores.
Pero non nos desviemos do tema.
O CO2 o que fai é que non permite que a radiación que entra na atmosfera procedente do Sol e rebota na superficie terrestre, volva saír o espacio, polo que aumenta a temperatura media da atmosfera.
Unha cousa ten que quedar clara, o efecto invernadoiro non se pode remediar, o que podemos e facer é que non siga en aumento.
Ben, comecemos polo principio.
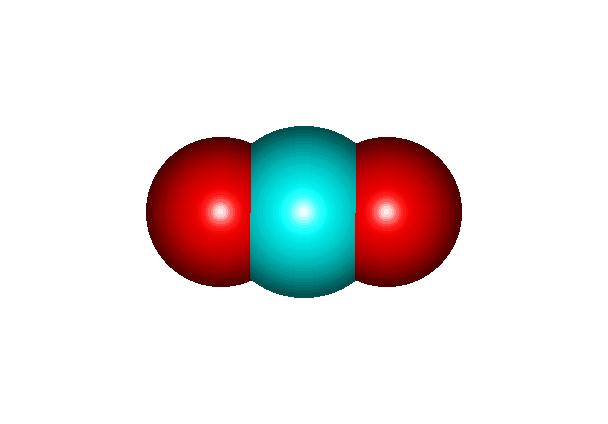
A fórmula química do dióxido de carbono é CO2.Aquí vos deixo unha pequena táboa coa súa nomenclatura sitemática, de stock e funcional.
FORMULACIÓN
A fórmula química do dióxido de carbono é CO2.Aquí vos deixo unha pequena táboa coa súa nomenclatura sitemática, de stock e funcional.

Como o CO2 é un óxido non metal pois para a súa nomenclatura sistemática comezamos "lendo" dende o final cara o principio.
Para a de Stock poñemos óxido de e o nome do metal. Entre parentesis poñemos a valencia coa que esta actuando.
Neste caso, como temos dous átomos de osíxeno, que actúa coa valencia 2- , o carbono ten que actuar con valencia 4+.
Para a nomenclatura tradicional poñemos a palabra Anhídrido e a continuación a raíz do nome do metal (carbon) e máis o sufixo ico, xa que este metal esta a actuar co número de oxidación máis elevado. Como o carbono ten valencias 2+ e 4+, se actuase con 2+, a menor, poriamos o sufixo -oso.
DATOS SOBRE O DIÓXIDO DE CARBONO
O CO2 atopámolo en estado gas na natureza, xa que ten unha temperatura de ebolución de - 78ºC.
Ten unha masa molecular de 44.01 umas (unidade de masa atómica), que se calula sumando as masas dos átomos que forman a molécula (neste caso, 12.01 do carbono máis 2x16 do osíxeno, xa que temos dos átomos)
CONSECUENCIAS CO2
O CO2 non é precisamente un gas moi bo para a nosa salud nin para o planeta Terra.
Quizais sexa menos peligroso ixestalo que inhalalo (quero dicir que dentro do malo, é menos malo comelo que respiralo, aínda que ambalas dúas cousas son perigosas)
Se tragamos CO2, cousa un pouco dificililla debido a que para ilo, precisaríamos atoparnos a menos de -78ºC baixo cero, provocaríanos nauseas, vómitos e tamén pupita na garganta.
Pero en vez diso, o que si que é moito máis doado de facer é inhalalo, como fixeron os xaponeses durante un tempo, que xuntábanse tres ou catro, metíanse nun coche coas ventanillas pechadas e levaban un tubo dende o tubo de escape ata o interior, de maneira que morrían ó certo tempo, pero iso si, morrían felices, porque o CO2 facía que se durmisen antes de morrer.
Aínda que atopei nunha páxina, que o CO2 non mata. Aquí vos deixo o link:
http://antonuriarte.blogspot.com/2007/01/el-co2-no-mata.html
Creo que o que eu entendín diso non é o que quere dicir, pero ven sendo que no noso alento, hai máis dióxido de carbono que na atmosfera actual.
Pero imos co que esta máis de moda: o cambio climático.
Aínda que non toda a culpa do cambio climático a ten o anhídrido carbónico, gran parte si. Veamos porque.
O CO2 é o gas máis importante dos que provoca o chamado efecto invernadoiro. Contribue nun 55% o calentamento global. Principalmente procede da quema de combustibles fósiles e da deforestación, porque aínda que pareza mentira, as árboles e as plantas, son capaces de transformar o dióxido de carbono en osíxeno.

Unha das causas que me levou a escribir sobre este composto é que o outo día, no programa de Cuatro "El Hormiguero", fixeron unha proposta.
Invitaron a todo o mundo a que plantase unha árbore e se seacase unha foto xunto a ela, Todo isto para loitar contra o efecto invernadoiro. Parece mentira, pero en 13 semanas, xa levan plantados 39.757 árbores.
Pero non nos desviemos do tema.
O CO2 o que fai é que non permite que a radiación que entra na atmosfera procedente do Sol e rebota na superficie terrestre, volva saír o espacio, polo que aumenta a temperatura media da atmosfera.
Unha cousa ten que quedar clara, o efecto invernadoiro non se pode remediar, o que podemos e facer é que non siga en aumento.
Publicado por
il Giorgio
en
3:21
![]()
-O AUGA-
0 comentarios(entrada publicada por Daniel Meira)
Quimicamente, o auga é un composto formado por dous átomos de hidróxeno e un de osíxeno.A sua fórmula é a coñecida H2O.

O auga cubre o 72% da Terra e representa entre o 50% e o 90% dos seres vivos. Podese encontrar esta substancia en case todalas biosferas, e en calquera dos tres estados:sólido, líquido, ou gasoso.
CARACTERISTICAS:O auga non ten nin olor, nin sabor, nin color.Chamaselle auga destilada á auga que foi evaporada e posteriormente condensada. O realizar este proceso eliminanse case todalas substancias disoltas e microorganismos que acostuma a conter a auga.
· o seu de ebullición é de 100ºC a presión dunha atmósfera.
· o seu punto de fusión é de 0ºC a presión dunha atmósfera.
· o auga pura non conduce a electricidade.
· o auga é un líquido casi incoloro, inodoro e insípido.
· pode estar en estado sólido, líquido ou gasoso.
· ten unha densidade de 1 g/cm3 a presion dunha atmósfera.
· ten unha tensión superficial moi elevadá.
· posee capilaridade, que é a propiedade de ascenso ou descenso dun líquido dentro dun cubo capilar.
· o calor latente de fusión do xeo (defínese como a cantidade de calor que necesita un gr de hielo para pasar de sólido a líquido, mantendo a temperatura constante no punto de fusión) a 0ºC: 80 cal/g.
· o calor latente de evaporación de auga a 100ºC: 540 cal/g.
· cristalízase en forma de neve
· ten un estado de sobreenfriado, é dicir, líquido a -25ºC.
· axuda a regular a calor dos animais
· proporciona flexibilidade ós texidos
· ten unha gran forza de cohesión entre as suas moléculas
 ·PROPIEDADES QUÍMICAS·
·PROPIEDADES QUÍMICAS·· non posee propiedades ácidas nin básicas.
· con certas sales forma hidratos.
· reacciona cós óxidos metálicos formando bases.
· é catalizador en moitas reacciones químicas.
...
-OS TRES ESTADOS DA AUGA-
-OS TRES ESTADOS DA AUGA-
ESTADO SÓLIDO: o estar a auga en estado sólido, todalas moléculas encóntranse unidas mediante un enlace de hidróxeno, que é un enlace intermolecular e forman unha estructura parecida á dun panal de abellas, o que explica que a auga neste estado sexa menos densa que en estado líquido. As moléculas están practicamente inmobiles. A auga o conxelarse aumenta o seu volume e baixa a sua densidade.
ESTADO LÍQUIDO:cando a auga esta en estado sólido, o ter mais temperatura, aumenta a enerxía das moléculas , entón o movemento das moléculas é maior.
Espero que a entrada fora do voso agrado, ata a semana que ven!
Publicado por
il Giorgio
en
8:16
![]()
Suscribirse a:
Comentarios (Atom)
Diseño e iconos por N.Design Studio | A Blogger por Blog and Web